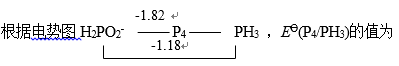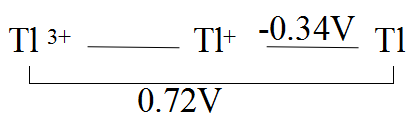下列氧化剂中, 其氧化性随 c (H+ )的增大而增强的是
A Ag+
B O2
C Cl2
D Cr2O72-
(2)单选题铜锌原电池的标准电极电势为1.11V,现有一铜锌原电池的电动势为1.17V,则该电池中Cu2+与Zn2+浓度比为
A 1:10
B 1:100
C 10:1
D 100:1
(3)单选题向由Ag+/Ag和Zn2+/Zn组成的原电池正负极溶液中加入氨水,达平衡后[NH3·H2O]=1mol·L-1,已知:K稳[Zn(NH3)4]2+=2.9×109,
K稳[Ag(NH3)2]+=1.1×107,与未加氨水时相比,原电池的电动势
A 变大
B 变小
C 不变
D 无法判断
(4)多选题对于电池反应Cu2+ + Zn = Zn2+ + Cu,欲使其电动势增大,可采取的措施有
A 降低 Zn2+浓度
B 增大Zn2+浓度
C 增大Cu2+浓度
D 降低 Cu2+浓度
(5)多选题下列电对的电极电势与pH有关的是
A H2O2/H2O
B O2/OH-
C MnO2/Mn2+
D MnO4–/ MnO42–
(6)判断题在氧化还原反应中,如果两电对的电极电势差值越大,则反应越易进行,速率越快。
对于原电池反应:Cu + 2Ag+ = Cu2+ + 2Ag,当Ag+ 和Cu2+浓度均为1 mol·dm-3时,该电池的电动势为2EӨ (Ag+ / Ag) - EӨ(Cu2+ / Cu)。
(8)单选题对于金属M,EӨ(M2+/M) = -0.40 V,EӨ(M3+/M) = -0.04 V,则EӨ(M3+/ M2+)的值为
A 0.96 V
B 0.68 V
C -0.44 V
D 1.00 V
(9)单选题已知EӨ( I2/I-) = 0.5355 V,EӨ(H2O2/H2O) = 1.776 V,EӨ(Cl2/Cl-) =1.3585 V, EӨ(Na+/Na) = -2.71 V,则下面还原性最强的是
A Na+
B H2O
C Cl-
D I-
(10)判断题
A -0.9 V
B -0.97 V
C 1.07 V
D -0.89 V
(12)单选题由下列电势图可知298K时反应 3 Tl+ = Tl3+ + 2 Tl的平衡常数为
A 3.8×10-66
B 1.3×10-54
C 7.0×1030
D 2.1×1017
获取标准答案请阅读全文
未经允许不得转载!第十章作业【含答案】 化学概论